二、选择题:每题各有一个或两个正确答案.(本题共6道小题,每题2分,共12分)
17.(2分)(2013•青岛)学习化学的目的并不在于人人都要成为化学家,更重要的是学会用化学观点去分析、解决生产生活中的问题.下列说法中,正确的是( )
A. 进入久未开启的地窖,应先做灯火实验
B. 夜间发现液化气泄漏应先开窗通风,不能立即开灯
C. 重金属盐能使蛋白质变性,起到杀菌作用,因此可用重金属盐溶液浸泡海产品
D. 海底蕴藏着大量“可燃冰”,以它为燃料不会对自然界中的碳循环产生影响
考点: 二氧化碳的化学性质;防范爆炸的措施;资源综合利用和新能源开发;常见中毒途径及预防方法.
专题: 化学与生活.
分析: A、二氧化碳不支持呼吸和燃烧,含量过高对人体有害;
B、根据液化气具有可燃性,与空气充分接触,遇电火花可能会产生爆炸分析;
C、根据重金属盐有毒,不能用重金属盐溶液浸泡海产品分析;
D、根据、“可燃冰”是天然气水合物,它的主要成分是甲烷,甲烷燃烧生成二氧化碳分析.
解答: 解:A、久未开启的地窖中可能含有较多的二氧化碳,二氧化碳不支持呼吸和燃烧,含量过高对人体有害,因此进入久未开启的地窖,应先做灯火实验,故A说法正确;
B、液化气具有可燃性,与空气充分接触,遇电火花可能会产生爆炸,开灯产生的电火花会引燃泄漏的液化气,因此夜间发现液化气泄漏应先开窗通风,不能立即开灯,故说法正确;
C、重金属盐能使蛋白质变性,起到杀菌作用,但是不能用重金属盐溶液浸泡海产品,因为吃了后易导致中毒,故C说法错误;
D、“可燃冰”是天然气水合物,它的主要成分是甲烷,甲烷燃烧生成二氧化碳,因此以“可燃冰”为燃料会对自然界中的碳循环产生影响,故D说法错误.
故选AB.
点评: 本题考查了常见物质的性质和用途,完成此题,可以依据已有的知识进行.
18.(2分)(2013•青岛)逻辑推理是化学学习中常用的思维方法.下列推理正确的是( )
A. 中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B. 化合物是由不同元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物
C. 单质中只含有一种元素,所以只含有一种元素的物质一定是单质
D. 活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属
考点: 中和反应及其应用;酸的化学性质;单质和化合物的概念.
专题: 结合课本知识的信息.
分析: A、中和反应特指的酸碱之间的反应,可以据此解答该题;
B、根据化合物的定义进行解答;
C、根据单质的定义进行判断;
D、活泼金属可以和稀硫酸反应生成气体,碳酸盐也可以和稀硫酸反应生成气体,可以据此解答该题.
解答: 解:A、中和反应特指的酸碱之间的反应,酸碱反应生成盐和水,但是生成盐和水的反应不一定是中和反应,例如二氧化碳和氢氧化钠反应生成了盐和水,但是它不属于中和反应,故A错误;
B、化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物,故B正确;
C、单质是由同种元素组成的纯净物,在叙述单质的定义时必须强调是纯净物,否则不成立,例如氧气和臭氧的混合物是由氧元素组成的,但是它属于混合物,而不是单质,故C错误;
D、活泼金属可以和稀硫酸反应生成气体,碳酸盐也可以和稀硫酸反应生成气体,故D错误.
故选B.
点评: 本题考查了学生在熟悉所学知识的基础上进行知识的整合归纳的能力,这就要求学生把握推理这一常用的学习方法,但推理时要特别注意一些特例的存在.通过回答本题可知有些知识要严格按照定义去推断,不能简单看表面现象.要从概念的实质出发去分析问题,解答此类题可用举反例的方法解决.
19.(2分)(2013•青岛)除去下列各物质中少量杂质的方法,不合理的是( )
选项 | 物质 | 所含杂质 | 除去杂质的办法 |
A | CO2 | CO | 通过足量的灼热氧化铜 |
B | N2 | O2 | 通过足量的灼热铜网 |
C | H2 | 水蒸气 | 通过盛有足量浓硫酸的洗气瓶 |
D | CO2 | HCl | 通过盛有足量氢氧化钠溶液的洗气瓶 |
A. A B. B C. C D. D
考点: 物质除杂或净化的探究.
专题: 物质的分离、除杂、提纯与共存问题.
分析: 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答: 解:A、CO能与灼热氧化铜反应生成铜和二氧化碳,二氧化碳不能与灼热氧化铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确.
C、浓硫酸具有吸水性,且不与氢气反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则;故选项所采取的方法错误.
故选D.
点评: 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.
20.(2分)(2013•青岛)下列图象能正确反映其对应关系的是( )
A.
某温度下,向一定量接近饱和的硝酸钾溶液中不断加入过量的硝酸钾晶体
B.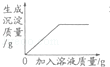
向稀盐酸和硫酸钠的混合溶液中加入过量的氢氧化钡溶液
C.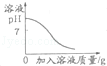
向氢氧化钠溶液中滴加过量的稀盐酸
D.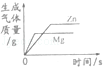
等质量的镁和锌同时分别放入两份溶质质量分数相同的足量稀盐酸中
考点: 饱和溶液和不饱和溶液;金属的化学性质;碱的化学性质;中和反应及其应用.
专题: 元素化合物知识型.
分析: A、根据饱和溶液的定义来进行解答;
B、氢氧化钡先与盐酸反应,再与硫酸钠反应生成沉淀;
C、根据酸碱发生中和反应进行判断;
D、等质量的镁和锌与足量酸反应产生氢气的多少进行判断
解答: 解:A、开始硝酸钾溶液不饱和,加入硝酸钾会溶解,溶质质量分数增加,硝酸钾溶液已饱和,所以再加入硝酸钾固体,硝酸钾不会溶解,所以溶质的质量分数也不会改变,故A错;
B、氢氧化钡先与盐酸反应,再与硫酸钠反应生成沉淀,所以开始没有沉淀生成,故B错;
C、在没加入盐酸前,溶液是氢氧化钠,pH值大于7,随着加入盐酸,pH值减小,当刚好反应完,pH值等于7,再加入盐酸,溶液会显酸性,pH值小于7,故C正确;
D、等质量的镁和锌与足量盐酸反应产生氢气的质量是:镁产生的氢气大于锌产生的氢气,故D错.
故选C.
点评: 解答这类题目时,首先,要熟记饱和溶液不饱和溶液的概念中和反应等;然后,根据所给的问题情景及相关信息,结合所学的相关知识和技能,联系起来细心地探究、推理后,按照题目要求进行选择或解答即可.
21.(2分)(2013•青岛)在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入等质量、等溶质质量分数的稀硫酸,将天平调节至平衡.然后向左盘的烧杯中加入8.4g铁,反应物之间恰好完全反应.欲使天平恢复平衡,则可向右盘的烧杯中加入( )
A. 8.4g铝 B. 8.4g氧化钙 C. 8.4g镁 D. 8.4g碳酸镁
考点: 根据化学反应方程式的计算.
专题: 有关化学方程式的计算.
分析: 可以用差量法进行计算,左盘烧杯中增加的质量和右盘烧杯中增加的质量相等时,天平保持平衡.
解答: 解:设与8.4g铁反应的硫酸的质量为X,生成氢气的质量为Y,
Fe+H2SO4═FeSO4+H2↑
56 98 2
8.4g X Y
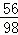 =
=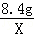
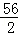 =
=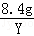
X=14.7g,Y=0.3g.
由计算可知,当向左盘的烧杯中加入8.4g铁时,生成0.3g氢气,左盘中实际增加的质量为:8.4g﹣0.3g=8.1g;
A、当加入8.4g铝时,铝过量,应该以硫酸的质量计算生成氢气的质量,
解:设加入8.4g铝时,生成氢气的质量为X,
2Al+3H2SO4═Al2(SO4)3+3H2↑
294 6
14.7g X
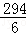 =
=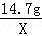
X=0.3g,
由计算可知,当向右盘的烧杯中加入8.4g铝时,生成0.3g氢气,右盘中实际增加的质量为:8.4g﹣0.3g=8.1g;
B、当向右盘的烧杯中加入8.4g氧化钙时,反应后没有气体逸出,右盘中实际增加的质量为8.4g;
C、当加入8.4g镁时,镁过量,应该以硫酸的质量计算生成氢气的质量,
解:设加入8.4g镁时,生成氢气的质量为X,
Mg+H2SO4═MgSO4+H2↑
98 2
14.7g X
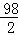 =
=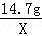
X=0.3g,
由计算可知,当向右盘的烧杯中加入8.4g镁时,生成0.3g氢气,右盘中实际增加的质量为:8.4g﹣0.3g=8.1g;
D、当加入8.4g碳酸镁时,硫酸过量,应该以碳酸镁的质量计算生成二氧化碳的质量,
解:设加入8.4g碳酸镁时,生成二氧化碳的质量为X,
MgCO3+H2SO4═MgSO4+H2O+CO2↑
84 44
8.4g X
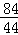 =
=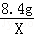
X=4.4g,
由计算可知,当向右盘的烧杯中加入8.4g碳酸镁时,生成4.4g二氧化碳,右盘中实际增加的质量为:8.4g﹣4.4g=4.0g;
由以上计算可知,欲使天平恢复平衡,则可向右盘的烧杯中加入8.4g铝或8.4g镁.
故选:AC.
点评: 本题较难,考查的内容较多,需要考虑多方面的知识,要运用多种方法计算.
22.(2分)(2013•青岛)我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )
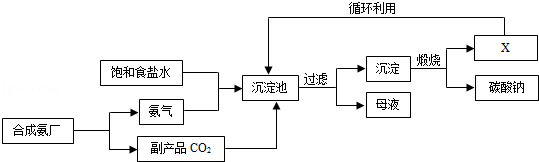
A. 沉淀池中的反应物共含有六种元素
B. 过滤得到的“母液”中一定只含有两种溶质
C. 图中X可能是氨气
D. 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀
考点: 纯碱的制取.
专题: 常见的盐 化学肥料.
分析: A、根据沉淀池中发生的反应是氯化钠、氨气、二氧化碳和水,再分析元素种类即可;B、过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的反应物;C、根据碳酸氢钠受热分解的生成物考虑;D、根据氨气的水溶液显碱性考虑.
解答: 解:A、沉淀池中发生的反应的反应物是氯化钠、氨气、二氧化碳和水,所以含有钠、氯、氮、氢、碳、氧六种元素,故A正确;
B、过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的氯化钠,故B错;
C、碳酸氢钠分解生成碳酸钠、水、二氧化碳,所以X是二氧化碳,故C错;
D、氨气的水溶液显碱性,能更好的吸收二氧化碳,使反应物浓度大,反应速度快,故D正确.
故选AD.
点评: 解答本题关键是要知道沉淀池中发生的反应,熟悉碳酸氢钠受热分解的产物,知道考虑反应后溶液中溶质时,还需要考虑反应物是否过量问题.












