三、实验题(共2个小题,每空1分,共14分)
12.(9分)(2013•黔西南州)化学实验里,老师给学生准备了如图几种实验装置.
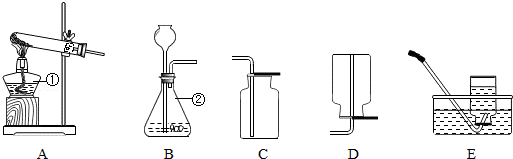
(1)指出仪器的名称:① 酒精灯 ② 锥形瓶 ;
(2)实验室用高锰酸钾制取氧气时,选择的发生装置和收集装置为 AC或AE ,反应的化学方程式为 2KMnO4 K2MnO4+MnO2+O2↑ ,属于 分解 反应(填基本反应类型);
K2MnO4+MnO2+O2↑ ,属于 分解 反应(填基本反应类型);
(3)实验室常用大理石与稀盐酸反应制取二氧化碳气体,选择的发生装置和收集装置为 BC ,反应的化学方程式为 CaCO3+2HCl═CaCl2+H2O+CO2 ↑ ;
(4)NH3是一种极易溶于水的气体,实验室常用加热NH4Cl和Ca(OH)2两种固体混合物来制取NH3,应选用的发生装置为 A ,反应的化学方程式为 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O .
2NH3↑+CaCl2+2H2O .
考点: 常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
专题: 压轴实验题;常见气体的实验室制法、检验、干燥与净化.
分析: (1)据常用仪器回答;
(2)实验室制取气体,发生装置的选择要看反应物的状态和反应条件;当反应物是固体,反应需要加热时,用A装置;当反应物是固体和液体,反应不需要加热时,用B装置;收集装置的选择要看气体的密度和溶解性.当气体比空气的密度大时,用向上排气法收集;当气体的密度比空气的密度小时,用向下排气法收集.当气体不溶于水时,用排水法收集;并据高锰酸钾制取氧气的反应原理书写方程式,据反应特点分析反应类型;
(3)实验室制取二氧化碳用大理石和稀盐酸,故应选择不需加热的B装置,二氧化碳能溶于水,比空气的密度大,因此收集气体时只能用向上排气法,并据反应原理书写方程式;
(4)实验室用加热NH4Cl和Ca(OH)2固体混和物的方法制取氨气并生成CaCl2和水,并据反应原理写出化学方程式.
解答: 解:(1)熟记常见仪器即可得出答案:①酒精灯;②锥形瓶;
(2)用高锰酸钾制取氧气,反应物是固体,反应需要加热,故选择发生装置A,氧气比空气的密度大,且不易溶于水,故可用向上排空气法或排水法收集,反应方程式是:2KMnO4 K2MnO4+MnO2+O2↑,该反应由一种物质生成三种物质,属于分解反应;
K2MnO4+MnO2+O2↑,该反应由一种物质生成三种物质,属于分解反应;
(3)实验室用碳酸钙和稀盐酸反应制取气体,反应物是固体和液体,反应不需加热,故选择发生装置B,二氧化碳气体比空气的密度大,且能溶于水.故用向上排空气法收集,反应的化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2 ↑;
(4)加热NH4Cl和Ca(OH)2固体混和物的方法制取氨气,故选择发生装置A,NH4Cl和Ca(OH)2两种固体混合物加热生成氨气、氯化钙和水,反应方程式是:2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O;
2NH3↑+CaCl2+2H2O;
故答案为:(1)酒精灯;锥形瓶;
(2)AC或AE;A; C或者E; 2KMnO4 K2MnO4+MnO2+O2↑;分解;
K2MnO4+MnO2+O2↑;分解;
(3)BC;CaCO3+2HCl═CaCl2+H2O+CO2 ↑;
(4)A;2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O.
2NH3↑+CaCl2+2H2O.
点评: 本题重点考查了装置选取方法和反应方程式的书写,发生装置的选择要看反应物的状态和反应条件,收集装置的选择要看气体的密度和溶解性.
13.(5分)(2013•黔西南州)烧杯中装有一定量的Na2CO3溶液,向其中加入一定量的CaCl2溶液,充分反应后过滤,得到滤渣和滤液,现对滤液中溶质的成分进行探究:
【提出猜想】:
猜想1 滤液中的溶质为NaCl;
猜想2 滤液中的溶质为NaCl、CaCl2;
猜想3 滤液中的溶质为 NaCl、Na2CO3 ;
猜想4 滤液中的溶质为NaCl、CaCl2、Na2CO3;
(1)完成猜想3.
(2)同学们一致认为,猜想4有明显的错误,其原因是 碳酸钠和氯化钙会 发生化学反应,不能同时存在 .
发生化学反应,不能同时存在 .
【设计实验,验证猜想】:
实验步骤 | 实验现象 | 实验结论 |
取滤液于试管中,向滤液中滴加适量的Na2CO3溶液 | (3) | 猜想2成立 |
取滤液于试管中,向滤液中滴加适量的稀盐酸 | (4) | 猜想3成立 |
【反思与评价】:
(5)当NaCl溶液中混有少量的Na2CO3溶液时,可选用下列哪些试剂除去Na2CO3杂质(多选题) ABC .
A.稀盐酸 B.CaCl2溶液 C.BaCl2溶液 D.Ba(OH)2溶液.
考点: 盐的化学性质;酸的化学性质.
专题: 压轴实验题;常见的盐 化学肥料.
分析: 根据物质的性质进行分析,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,如果反应物过量,则存在剩余的情况;碳酸盐遇酸化气;除去杂质时不能产生新的杂质,据此解答.
解答: 解:猜想3、碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,如果反应物过量,则存在剩余的情况,若碳酸钠过量,则含有的溶质是氯化钠和碳酸钠,故填:NaCl、Na2CO3;
(2)由于碳酸钠和氯化钙混合会发生反应生成碳酸钙沉淀,剩余碳酸钠和氯化钙不会同时剩余,故填:碳酸钠和氯化钙会发生化学反应,不能同时存在;
(5)要除去氯化钠中混有的碳酸钠,所加入的试剂与碳酸钠反应不能生成新的杂质,盐酸和碳酸钠反应生成氯化钠和税以及氯化钠,不引入新的杂质,使用盐酸可以除去碳酸钠;氯化钙溶液和碳酸钠反应生成碳酸钙沉淀和氯化钠,不引入新的杂质,可以使用氯化钙溶液除去碳酸钠;氯化钡溶液与碳酸钠反应生成碳酸钡沉淀和氯化钠,不引入新的杂质,可以使用氯化钡除去碳酸钠;氢氧化钡与碳酸钠反应生成碳酸钡沉淀和氢氧化钠,引入新的杂质氢氧化钠,不能使用氢氧化钡除去碳酸钠,故填:ABC.
点评: 本题考查了混合物成分的推断以及杂质的去除方法,完成此题,可以依据物质的性质进行.
四、计算题(共6分)
14.(6分)(2013•黔西南州)一块表面被氧化的铝片质量为15.6g,将其放入烧杯中,加入213g稀硫酸,恰好完全反应,反应后,称得烧杯中的溶液质量为228g,求:(提示:Al2O3+3H2SO4═Al2(SO4)3+3H2O 2Al+3H2SO4═Al2(SO4)3+3H2↑)
(1)生成氢气的质量为 0.6 g;
(2)反应后所得溶液中溶质的质量分数.
考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
专题: 压轴实验题;溶质质量分数与化学方程式相结合的计算.
分析: (1)氧化铝与硫酸反应生成硫酸铝和水,铝和硫酸反应生成硫酸铝和氢气,由发生的反应原理可知,反应前后减少的质量是生成的氢气的质量;
(2)反应后所得溶液是硫酸铝溶液,根据生成氢气的质量可计算出铝的质量和硫酸与铝反应生成的硫酸铝的质量,氧化铝的质量就等于总质量﹣铝的质量,由氧化铝的质量计算出生成的氧化铝的质量,再根据溶质的质量分数计算即可.
解答: 解:(1)根据质量守恒定律可知,反应前后减少的质量是生成氢气的质量,为:15.6g+213g﹣228g=0.6g;
(2)设铝片中铝的质量是x,生成的硫酸铝的质量为y
2Al+3H2SO4═Al2(SO4)3+3H2↑
54 342 6
x y 0.6g
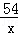 =
=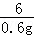 x=5.4g
x=5.4g
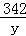 =
=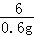 y=34.2g
y=34.2g
所以铝片中氧化铝的质量为:15.6g﹣5.4g=10.2g
设氧化铝反应生成的硫酸铝的质量为a
Al2O3+3H2SO4═Al2(SO4)3+3H2O
102 342
10.2g a
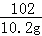 =
=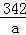
a=34.2g
反应后所得溶液中溶质的质量分数为: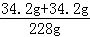 ×100%=30%
×100%=30%
故答案为:(1)0.6g;(2)反应后所得溶液中溶 质的质量分数为30%.
质的质量分数为30%.
点评: 本题考查了学生对于质量守恒定律的理解和应用,并能结合题目中化学反应原理灵活分析解答问题,尤其是反应后溶液中溶质的确定,要细心分析解答.












