14.(2分)(2013•永州)每年3月22日是“世界水日”,下列有关水的叙述正确的是( )
A. 经常饮用蒸馏水对身体有益
B. 可用肥皂水区别硬水和软水
C. 所有物质在水中的溶解度都随温度的升高而增大
D. 地球上的水资源丰富,取之不尽,用之不竭
考点: 硬水与软水;水资源状况;气体溶解度的影响因素.
专题: 空气与水.
分析: A、蒸馏水属于纯度最高的水,可看作是纯净物;
B、硬水中含有较多的钙、镁离子,与肥皂水作用时基本不产生泡沫或有较多的悬浮杂质,软水则相反;
C、氢氧化钙在水中的溶解度随温度的升高而减小;
D、水资源并不是取之不尽,用之不竭的.
解答: 解:A、蒸馏水属于纯度最高点水,可看作是纯净物,不含人体所需要的矿物元素,所以经常饮用蒸馏水对身体无益,故A错误;
B、硬水中含有较多的钙、镁离子,与肥皂水作用时基本不产生泡沫或有较多的悬浮杂质,软水则相反,故B正确;
C、大多数固体物质在水中的溶解度随温度的升高而增大,但是象气体、氢氧化钙固体等物质在水中的溶解度随温度的升高而减小,故C错误;
D、水资源并不是取之不尽,用之不竭的,故D错误.
故答案为B.
点评: 本题难度不大,了解水体污染的主要途径与谁资源的保护等即可正确解答本题.
15.(2分)(2013•永州)氢氧化钴[Co(OH)2]受热易分解,能与酸性溶液反应,可作涂料和清漆的干燥剂,制备方法为:①Co+2HCl=CoCl2+H2↑②CoCl2+2NaOH=Co(OH)2↓+2NaCl下列说法正确的是( )
A. 钴与金属铜的化学性质相同 B. 氢氧化钴难溶于水
C. 氢氧化钴的化学性质稳定 D. 氢氧化钴可用于干燥氯化氢气体
考点: 碱的化学性质;金属的化学性质;酸碱盐的溶解性.
专题: 结合课本知识的信息.
分析: 根据题干提供的化学方程式进行分析,钴能与盐酸发生反应;氢氧化钴属于碱,是不溶于水的物质,据此解答即可.
解答: 解:A、钴能与盐酸发生化学反应,而铜不与盐酸反应,故钴与铜的化学性质不相同,故A错误;
B、根据②可以看出,生成的氢氧化钴是沉淀,是难溶于水的物质,故B正确;
C、氢氧化钴受热易分解,其化学性质不稳定,故C错误;
D、氢氧化钴属于碱,不能用于干燥氯化氢气体,故D错误;
故选B.
点评: 本题为信息给予题,完成此题,可以依据题干提供的信息结合物质的性质进行.
16.(2分)(2013•永州)现有甲、乙、丙三种金属,将甲、乙两种金属分别放入相同浓度的稀硫酸中,乙表面产生气泡,甲表面无明显现象;将甲、丙分别放入AgNO3溶液中,甲表面有银析出,丙表面无明显现象.下列对甲、乙、丙三种金属活动性 顺序的排列正确的是( )
顺序的排列正确的是( )
A. 甲>乙>丙 B. 乙>丙>甲 C. 乙>甲>丙 D. 丙>甲>乙
考点: 金属活动性顺序及其应用.
专题: 金属与金属材料.
分析: 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢;位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此根据能否发生反应,可确定三种金属活动性由强到弱的顺序.
解答: 解:将甲、乙两种金属分别分别放入相同浓度的稀硫酸中,乙表面产生气泡,甲表面无明显现象,说明乙能与稀盐酸反应,甲不能与稀盐酸反应,即乙>H>甲;
将甲、丙分别放入AgNO3溶液中,甲表面有银析出,说明甲的金属活动性比银强,即甲>Ag;丙表面无明显现象,说明丙的金属活动性比银弱,即Ag>丙;
则甲、乙、丙三种金属的活动性由强到弱的顺序是乙>甲>丙.
故选C.
点评: 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.
17.(2分)(2013•永州)化学方程式是重要的化学用语.下列化学方程式书写正确的是( )
A. 2KMnO4 K2MnO4+MnO2+O2↑ B. S+O2
K2MnO4+MnO2+O2↑ B. S+O2 SO3
SO3
C. Cu+FeSO4=CuSO4+Fe D. CaCO3+HCl=CaCl2+H2O+CO2↑
考点: 书写化学方程式、文字表达式、电离方程式.
专题: 化学用语和质量守恒定律.
分析: 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
解答: 解:A、该化学方程式书写完全正确.
B、硫在氧气中燃烧生成二氧化硫,正确的化学方程式为:S+O2 SO2.
SO2.
C、铜的金属活动性比铁弱,不能与硫酸亚铁溶液发生反应,故该化学方程式错误.
D、该化学方程式没有配平,正确的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
故选A.
点评: 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断,化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.
18.(2分)(2013•永州)硝酸是一种具有强氧化性的酸,它不仅能与活泼金属发生反应,也能与许多不活泼金属发生反应.其中金属铜与稀硝酸反应的化学方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O,则X的化学式为( )
A. NO2 B. NO C. N2O D. N2O4
考点: 质量守恒定律及其应用.
专题: 化学用语和质量守恒定律.
分析: 根据反应的化学方程式3Cu+8HNO3(稀)=3Cu(NO3 )2+2X↑+4H2O,利用反应前后原子种类、数目不变,推断生成物X的化学式.
)2+2X↑+4H2O,利用反应前后原子种类、数目不变,推断生成物X的化学式.
解答: 解:从反应的化学方程式3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O看,反应前3Cu、8HNO3中含Cu、H、N、O四种元素的原子个数分别为3、8、8、24,反应后3Cu(NO3)2、4H2O中含Cu、H、N、O四种元素的原子个数分别为3、8、6、22,根据反应前后原子种类、数目不变,可判断2X中含2个N原子和2个O原子,则每个X分子由1个N原子、1个O原子构成,则物质X的化学式为NO;
故选B.
点评: 根据反应的化学方程式,利用反应前后原子种类、数目不变,可推断反应中某物质的分子构成、确定该物质的化学式.
19.(2分)(2013•永州)除去下列物质中的少量杂质(括号内为杂质),所选用的试剂和操作错误的是( )
选项 | 物质(杂质) | 选用试剂及操作 |
A | CaCO3(CaCl2) | 加水,将固体溶解后过滤 |
B | Cu粉(Fe粉) | 加过量稀盐酸,充分反应后过滤 |
C | KCl溶液(MgCl2) | 加适量NaOH溶液,过滤 |
D | CO2气体(水蒸气) | 将气体通入盛有浓硫酸的洗气瓶 |
A. A B. B C. C D. D
考点: 物质除杂或净化的探究;常见气体的检验与除杂方法;金属的化学性质;盐的化学性质.
专题: 压轴实验题;物质的分离、除杂、提纯与共存问题.
分析: 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答: 解:A、氯化钙易溶于水,碳酸钙难溶于水,可采取加水溶解、过滤的方法进行分离除杂,故选项所采取的试剂和操作正确.
B、铁粉能与稀盐酸反应生成氯化亚铁和氢气,铜不与稀盐酸反应,再过滤除去不溶物,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的试剂和操作正确.
C、MgCl2能与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项所采取的试剂和操作错误.
D、浓硫酸具有吸水性,且不与二氧化碳反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的试剂和操作正确.
故选C.
点评: 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.
20.(2分)(2013•永州)向100g质量分数为20%的NaCl溶液中加入3gNaCl固体和12g水,使其完全溶解,所得溶液中NaCl的质量分数是( )
A. 20% B. 22.5% C. 25% D. 30%
考点: 有关溶质质量分数的简单计算.
专题: 压轴实验题;溶液的组成及溶质质量分数的计算.
分析: 根据溶质的质量分数= 100%,结合题意进行分析解答.
100%,结合题意进行分析解答.
解答: 解:向100g质量分数为20%的NaCl溶液中加入3gNaCl固体和12g水,使其完全溶解,所得溶液中NaCl的质量分数是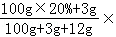 100%=20%.
100%=20%.
故选A.
点评: 本题难度不大,掌握溶质质量分数的有关计算并能灵活运用即可正确解答本题.
二、填空题(共6小题,每小题4分,满分30分)
21.(4分)(2013•永州)掌握化学用语是学好化学的基础工程,请你用相应的化学符号和数字填写下列空格.
(1)铝元素 Al
(2)2个氯原子 2Cl
(3)一个氮分子 N2
(4)+4价的碳元素 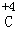 .
.
考点: 化学符号及其周围数字的意义.
专题: 化学用语和质量守恒定律.
分析: (1)书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写.
(2)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
(3)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(4)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.
解答: 解:(1)铝元素的元素符号为:Al.
(2)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氯原子表示为:2Cl.
(3)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则一个氮分子可表示为:N2.
(4)由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故+4价的碳元素可表示为: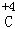 .
.
故答案为:(1)Al;(2)2Cl;(3)N2;(4)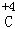 .
.
点评: 本题难度不大,主要考查同学们对常见化学用语(元素符号、原子符号、分子符号、化合价等)的书写和理解能力.
22.(4分)(2013•永州)现有①干冰②碳酸钙③甲烷④醋酸四种物质,请按照下列要求选用物质的序号填空:
(1)可用于人工降雨的是 ① ;
(2)医疗上常用作补钙剂的是 ② ;
(3)天然气的主要成分是 ③ .
考点: 二氧化碳的用途;碳酸钠、碳酸氢钠与碳酸钙;化石燃料及其综合利用.
专题: 物质的性质与用途.
分析: 物质的性质决定物质的用途,干冰是固态的二氧化碳,升华时吸收大量的热;碳酸钙在医疗上常用作补钙剂;天然气的主要成分是甲烷;据此进行分析解答.
解答: 解:(1)干冰是固体的二氧化碳,升华时吸收大量的热,可用于人工降雨.
(2)碳酸钙在医疗上常用作补钙剂.
(3)天然气的主要成分是甲烷.
故答案为:(1)①;(2)②;(3)③.
点评: 本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.












